כימיה לבגרות/ כימיה - תורת החומר : מושגי יסוד, הפרדת חומרים, מצבי צבירה וחלקיקים ומצב צבירתם
הקדמה – מהי כימיה? במה עוסקת?
[עריכה]כימיה — מדע העוסק בחומר ובתכונותיו.
[עריכה]
כימיה ענף מדע מרכזי במדעי הטבע העוסק בהרכב החומר, מבנהו, תכונותיו והשינויים החלים בו כשהוא בא במגע עם חומרים אחרים או בהשפעת כוחות פיזיקליים.
כמו תחומים נוספים במדעי הטבע היא מתקשרת וחופפת לתחומי מדע רבים, (כגון: אסטרונומיה, פיזיקה, מדע החומרים, ביולוגיה, גאולוגיה וכו'), תחומי הנדסה ותחומים מעשיים נוספים (כגון: רפואה, הנדסת חומרים, הנדסה חקלאית, יצור מזון, ביוטכנולוגיה וכו').
היסטוריה של הכימיה
[עריכה]מבחינה היסטורית, הכימיה המודרנית התפתחה מהאלכימיה בעקבות המהפכה הכימית (1773) אך ההיסטוריה של הכימיה מתחילה כבר לפני יותר מ-4,000 שנה במצרים העתיקה, שם החלו הנסיונות הראשונים בכימיה ניסויית (המכונה "כימיה רטובה", בניגוד לכימיה תאורטית).
בסביבות 1000 לפני הספירה החלו תרבויות שונות להשתמש בטכנולוגיות שלימים יהוו את הבסיס לענפי הכימיה המודרנית. הפקת מתכות מעפרות, קדרות וזכוכית, ייצור בירה ויין, ייצור פיגמנטים לשימושים קוסמטיים ולצביעה, צביעת בדים, עיבוד עורות, ייצור גבינה, מיצוי חומרים מצמחים למטרות רפואה ובשמים, יצירת מסגים ושימוש בשומן ליצירת סבון היו חלק מהתהליכים הכימיים הראשונים שנעשה בהם שימוש.
ניסיונות פילוסופיים לקביעת טבעו ומבנהו של החומר נכשלו, ואף ניסיונותיהם של האלכימאים לא צלחו, אך ניסויים אלה והתיעוד שהותירו אחריהם הכשירו את הדרך להתפתחות הכימיה המודרנית. נהוג לראות את סיום האלכימיה וניצניה של הכימיה המודרנית בעבודתו של רוברט בויל, The Sceptical Chymist ("הכימאי הסקפטי", בתרגום חופשי) שראתה אור בשנת 1661 בלונדון. עבודתו של אנטואן לבואזייה בנושא חוק שימור החומר, שדרשה מדידות ותצפיות מדויקות של תופעות כימיות, הפכה את הכימיה למדע מדויק. למעשה, גם הכימאים וגם האלכימאים עסקו בהרכב החומר, מבנהו והתגובות שהוא יוצר, אך ההבדל בהם טמון במטרותיהם ובעובדה שהכימאים עובדים לפי השיטה המדעית. ההיסטוריה של הכימיה משתלבת גם עם ההיסטוריה של התרמודינמיקה, בעיקר דרך עבודתו של וילארד גיבס.
תחילתה של הכימיה המודרנית הייתה בקבלתה של התורה האטומית,[1] ויצירת הטבלה המחזורית. עם התפתחות תורת הקוונטים נטשטשה החלוקה המסורתית הברורה בין פיזיקה לכימיה, ושתיהן חופפות בתחום של יצירה, אפיון ותכונות של חומרים ומולקולות, ואף חופפות לביולוגיה בחקר של נגיפים ותהליכים בתאים.
מושגי יסוד
[עריכה]הגדרת מושגים בסיסיים
[עריכה]חומר - חומר הוא כל דבר שיש לו מסה ותופס נפח במרחב.
בחומר אנו מתכוונים למושג האינטואיטיבי אותו אתה מכיר, החומרים השונים סביבנו מרכיבים את כל הסובב אותנו.
על פי התורה האטומית (העוסקת בטיבו של החומר), החומר עשוי מיחידות נפרדות ו־"סופיות", בניגוד לדעה עתיקה יותר, שלפיה ניתן לחלק את החומר ליחידות הולכות וקטנות, עד אינסוף. התורה האטומית החלה כרעיון פילוסופי ביוון העתיקה ובהודו, ונכנסה לזרם המרכזי במדע בראשית המאה ה-19, כאשר תגליות בתחום הכימיה הראו כי החומר אכן מתנהג כעשוי מחלקיקים.
לחלקיקים אלו אנו קוראים אטומים:
אטום - החלקיק הקטן ביותר של יסוד כימי שבו נשמרות תכונות היסוד הכימיות
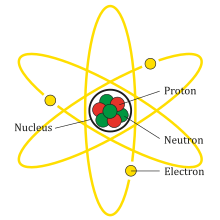
האטום (ביוונית: ἄτομος), שפירושו "לא ניתן לחיתוך" - "א" (לא ניתן) "טומי" (חתך) הוא החלקיק הקטן ביותר של יסוד כימי שבו נשמרות תכונות היסוד; לפי המודל הסטנדרטי האטום מורכב מחלקיקים קטנים יותר שאינם באים לידי ביטוי בתורה הכימית. שמו הוטבע במאה ה-5 לפנה"ס על ידי הפילוסוף היווני דמוקריטוס, שהניח את קיומו. כשהתגלה החלקיק במאה ה-18, רווחה הדעה שלפיה האטום הוא חלקיק יסודי שאינו ניתן לחלוקה לחלקיקים קטנים יותר. מאוחר יותר התגלה כי האטום מורכב מחלקיקים קטנים יותר: גרעין קטן וכבד שבו פרוטונים ונייטרונים, וסביבו ענן של אלקטרונים. הפרוטונים והנייטרונים עצמם מורכבים מחלקיקים נוספים.
גודלו של אטום נע בין 60 פיקו-מטר (מיליונית של מיליונית המטר - 0.000,000,000,001 מ') עבור אטום הליום ל-500 פיקו-מטר עבור אטום צסיום. אטומים הם קטנים מכדי לראותם בעין, אך קיימים מיקרוסקופים בעלי כושר אבחנה עדין מספיק כדי להבחין בהם, למשל מיקרוסקופ מינהור סורק, ואחרים המסוגלים לזהות את סוג האטום.

את האטומים השונים אנו מסווגים וממיינים לפי הטבלה המחזורית.
הטבלה המחזורית או המערכה המחזורית, המכונה גם טבלת מנדלייב, היא שיטת מיון שהוצעה לראשונה על ידי הכימאי הרוסי דמיטרי מנדלייב ב-1869, ומציגה את כל סוגי האטומים הקיימים (ואף כאלו מלאכותיים שלא נמצאים בטבע ומתקיימים במעבדות בלבד) ומייצגת אותם על ידי היסודות אותם המהרכיבים:
- יסוד - מצבור של אטומים זהים, למשל ברזל (Fe), מימן (H) ועוד.
יסוד כימי או בקיצור, יסוד, הוא חומר המורכב מחלקיקים אטומיים מסוג אחד בלבד. לא ניתן להרכיב יסוד מחומרים אחרים, לא ניתן לפרק יסוד או לשנותו ליסוד אחר בתהליכים כימיים, זאת בניגוד לתרכובת המורכבת מיסודות.
האטומים ביסוד מסודרים באחת מן הצורות: בצורה חד-אטומית, כמו במקרה של גזים אצילים, כמולקולה (ראה בהמשך) עם אטומים זהים בלבד, או כגביש (על כך בפרקים הבאים) של אטומים זהים בלבד.
כיום ידוע כי רוב החומרים מורכבים לא מסוג אחד של אטומים בלבד אלא ממולקולות, שהן מספר אטומים שקשורים זה לזה.
מולקולה – מבנה בן מספר אטומים המחוברים ביניהם בקשר כימי.
מוֹלקוּלה (מלטינית: Molecula - מסה קטנה; בעברית גם פּרוּדה) היא מונח בכימיה שנטבע על ידי הכימאי אמדאו אבוגדרו לתיאור מבנה בן מספר אטומים המחוברים ביניהם בקשר כימי. המולקולה היא יחידת בסיס (החלק הלא פריק הקטן ביותר) של תרכובת מולקולרית וניתן לומר כי מבנה המולקולה, הרכבה וכוחות המשיכה בין אטומיה קובעים את תכונות התרכובת. מולקולה עשויה להיות מורכבת ממספר אטומים זהים או שונים. למשל מולקולת חמצן (O2) המורכבת שני אטומים זהים, מולקולת סוכר המורכבת מעשרות אטומים שונים, או מולקולת DNA הבנויה מיליוני אטומים.
כדי לתאר מולקולות, באופן מדויק יותר, נהוג להשתמש בנוסחת המבנה של החומר או באיור.
סוגי חומרים
[עריכה]נבדיל בין מספר סוגי חומרים:
- תרכובת – מצבור של מולקולות זהות (להבדיל מייסוד, המולקולות מורכבות מסוגים שונים של אטומים, אך בהרכב קבוע).
- לתרכובת תכונות כימיות משל עצמה, השונות מתכונות מרכיביה. למשל, מלח בישול (NaCl), הוא תרכובת של המתכת, נתרן, והאל מתכת, כלור. לתרכובת הרכב קבוע ומוגדר של אטומים; הרכב זה ניתן על ידי הנוסחה של החומר. מספר התרכובות הידועות למדע הוא עצום. נכון ל-2006 ידועות למדע מעל ל-30 מיליון תרכובות שונות.
- חומר טהור - חומר שהוא תרכובת או יסוד (כלומר, חומר המורכב ממולקולות זהות, לא משנה אם מייסוד אחד או יותר, אבל בהרכב קבוע).
- תערובת - ערבוב של שניים או יותר חומרים טהורים, אך ללא קשר כימי ביניהם (כלומר היא מכילה מספר סוגי מולקולות) כשכל חומר שומר על תכונותיו, למשל: אוויר (מכיל: 78% חנקן, 21% חמצן, 1% ארגון, 0.03% פחמן דו-חמצני ועוד) או בוץ - תערובת של מים עם חומר (סיליקט) וחומרים אחרים הנמצאים באדמה.
ישנם שני סוגי תערובות:- הומוגנית– ערבוב שאינו נראה לעין. המילה הומו פרושה שווה מצב שבו מס החומרים שאינם קשורים בקשר כימי יוצר תערובת אחידה שלא ניתן להבחין בין מרכיביה. למשל: פטל + מים.
- הטרוגנית – תערובת שאפשר להבחין בין מרכיביה השונים, שאינה אחידה.
חשוב מאוד להבדיל תרכובת לתערובת !
- סמלים של יסודות - לכל יסוד מהטבלה המחזורית ניתן סמל. הסמלים מורכבים מאותיות לטיניות. סמלו של כל יסוד מורכב מאות אחת עד שלוש אותיות. לרוב הסמלים מהווים קיצור של שמו הלטיני של היסוד. לדוגמא הסמל של ברזל הוא Fe. סמל זה בא משמו הלטיני של היסוד - פרום.
- נוסחה כימית - משמשת להצגת תרכובת.
מושגי יסוד בהרחבה
[עריכה]יסוד כימי
[עריכה]יסוד כימי, בקיצור יסוד, הוא חומר המורכב מחלקיקים אטומיים מסוג אחד בלבד. לא ניתן להרכיב יסוד מחומרים אחרים, לא ניתן לפרק יסוד לחומרים אחרים או לשנותו ליסוד אחר בתהליכים כימיים (לא גרעיניים), זאת בניגוד למולקולה המורכבת מיסודות. היסודות נבדלים זה מזה במספר הפרוטונים בגרעין; מספר זה הוא המספר האטומי.
חומר טהור
[עריכה]חומר העשוי סוג יחיד של מולקולות או יסודות ולא סוגים שונים של מולקולות.
תרכובות
[עריכה]תרכובת היא חומר הבנוי משני סוגי יסודות או יותר, הקשורים ביניהם בקשר כימי כלשהו וביחס קבוע של כמויותיהם. לתרכובת תכונות כימיות משל עצמה, השונות מתכונות מרכיביה. יש להבדיל בין תרכובת לבין תערובת, המכילה מספר אטומים או תרכובות יחדיו, אך ללא קשר כימי ביניהם, כך שכל חומר שומר על תכונותיו הכימיות והיחס בין מרכיביה אינו בהכרח קבוע. תמיסה, למשל, היא תערובת.
תערובות
[עריכה]תערובת היא חומר המכיל מספר חומרים שונים: יסודות, תרכובות או שניהם יחד, השומרים על תכונותיהם הכימיות והפיזיקליות. תרכובת גם היא מורכבת מחומרים שונים, אך הללו קשורים ביניהם בקשרים תוך-מולקולריים, דבר המקנה לתרכובת תכונות עצמאיות משלה, אשר בדרך כלל שונות מאוד מהתכונות של החומרים המרכיבים אותה. ישנם שני סוגים של תערובות: תערובת הומוגנית (אחידה) ותערובת הטרוגנית (לא אחידה).
- תערובת הומוגנית - תערובת הומוגנית היא תערובת שבה אי אפשר להבחין בין מרכיבי התערובת, גם מבעד למיקרוסקופ אופטי; תערובת הומוגנית נקראת גם בשם תמיסה, לדוגמה: סגסוגת.
- תערובת הטרוגנית - בתערובת הטרוגנית ניתן להבדיל בין מרכיבי התערובת; לדוגמה: סלט, או חלב, בו ניתן להבחין בטיפות שומן צפות. קיימות גם תערובות הטרוגניות שלא ניתן להבחין בין מרכיבי התערובות מחמת קוטנם, אולם ניתן להבחין בהם באמצעים אופטיים.
לתערובות יש שמות שונים לפי מצבי הצבירה של החומרים בהן. תחליב הוא תערובת דמוית חלב, של נוזל שומני בנוזל המתערבב במים בקלות. סוג זה של תערובת נוטה להיפרד בקלות. החלב התעשייתי, להבדיל מחלב ישירות מן הפרה, עובר תהליך המגון אשר מיועד לאחד את מרכיבי החלב לידי תערובת אחידה. לאחר הקפאה עשוי החלב להיפרד למרכיביו. תרחיף הוא תערובת של אבקה בנוזל. תרופות ילדים רבות (סירופים) משווקות באופן זה. גם סוג זה של תערובת נוטה להיפרד, ודרוש ניעור לפני השימוש בתרופה.
הסגסוגת היא תערובת מתכות, אשר אינה נוטה להיפרד בנקל. אטומי כל מתכת מסודרים עדיין בגרעינים שלמים בתוך הסגסוגת. גרעיני המתכת מהווים גבישים זעירים, שבתוכם דומה מבנה המתכת למבנה הרגיל שלה, כאשר היא טהורה. אך הגרעינים משולבים אלה באלה במבנה חזק ויציב.
מולקולה
[עריכה]מולקולה היא החלק הקטן ביותר של כימיקל טהור השומר על תכונותיו הכימיות, כלומר, היכולת לעבור סדרת תגובות כימיות מוגדרת עם כימיקלים אחרים. מולקולות יכולות להיות נייטרליות מבחינה חשמלית בניגוד ליונים. המולקולות הן בדרך כלל קבוצה של אטומים הקשורים בקשר קוולנטי, כך שהמבנה הכולל נותר נייטרלי מבחינה חשמלית, וכל אלקטרוני הקשר מזווגים עם אלקטרונים אחרים בקשר כימי או נמצאים במולקולה כאלקטרונים בלתי קושרים.
אחת מהתכונות העיקריות של מולקולה היא הגאומטריה שלה המכונה לעתים גאומטריה מולקולרית. בעוד שהמבנה של מולקולות דו-אטומיות, תלת-אטומיות וארבע-אטומיות עשוי להיות טריוויאלי (קווי, זוויתי או פירמידה), המבנה של מולקולות רב-אטומיות, שהן מולקולות המורכבות מ-6 אטומים ומעלה (או מספר יסודות שונים), עשוי להשפיע במידה רבה על מאפייניה הכימיים.
אטום
[עריכה]אטום הוא היחידה הבסיסית של יסוד כימי. האטום הוא אוסף של חלקיקי חומר המורכב מליבה טעונה במטען חשמלי חיובי (גרעין האטום) המכילה פרוטונים ונייטרונים, שאותה מקיפים אלקטרונים הנושאים מטען חשמלי שלילי ומאזנים את המטען החיובי שבגרעין. אטום הוא החלק הקטן ביותר של החומר ששומר על התכונות הכימיות של היסוד.
חוק שימור החומר וישומו
[עריכה]חומר לא נוצר יש מאין, אך הוא יכול להתגלגל בין מצבי צבירה שונים ולהוות פוטנציאל לאנרגיה (שהיא כאמור איננה חומר).
הפרדה בין חומרים
[עריכה]חומרים ניתנים להפרדה על ידי שתי דרכים:
- הפרדה על ידי תכונות פיסיקאליות - משמש לפירוק תערובות. כאשר מערבבים חומרים שונים, כל חומר שומר על התכונות הקבועות שלו ולכן ניתן לפרק את התערבות בתהליך פיזיקאלי שלא פוגע בתרכובות שמרכיבות את התערובת. לדוגמא, כדי לפרק תערובת של מים וחול, מאדים את המים (על ידי הרתחה) ואז החול והמים מופרדים.
- הפרדה על ידי תכונות כימיות - כאשר קיים קשר כימיים בין שני חומרים הוא מתבצע על ידי שריפה (חמצון), התרכבות ופירוק.
הערות שוליים
[עריכה]- ^ המושגים המודגשים לאורך העמוד יובהרו בהמשך.






